Mit der fortschreitenden Digitalisierung im Gesundheitswesen geraten Krankenhaus-informationssysteme (KIS) zunehmend in den regulatorischen Fokus. Unter der EU-Medizinprodukteverordnung (MDR) stellt sich dabei die Frage, wann ein KIS als „System“ oder „Behandlungseinheit“ gilt – mit direkten Auswirkungen auf Compliance und Betreiber-verantwortung. Eine Einordnung dazu liefert das Johner Institut:
Krankenhausinformationssysteme (KIS) zählen zu den klinischen Informationssystemen. Als zentraler Teil der IT-Infrastruktur von Krankenhäusern dienen sie der digitalen Verwaltung und Verarbeitung sämtlicher administrativer und medizinischer Patientendaten in einem Krankenhaus. Ein KIS fungiert als elektronische Patientenakte und steuert Prozesse: von der Aufnahme über Diagnose und Behandlung bis zu Entlassung und Abrechnung.
Dieser Artikel beleuchtet unter Berücksichtigung der EuGH-Entscheidung vom 07.12.2017 (C-329/16) die Frage, ob ein KIS, das Medizinprodukte-Module enthält, als System oder als Behandlungseinheit zählt.
Key Takeaways
- Nur medizinische Module brauchen eine CE-Kennzeichnung. Der EuGH hat klargestellt: Enthält eine Software sowohl medizinische als auch nicht-medizinische Module, müssen nur die medizinischen Module „zertifiziert“ werden – vorausgesetzt, Grenzen und Schnittstellen sind klar definiert.
- Ein KIS ist in der Regel kein „System“ und keine „Behandlungseinheit“ i. S. d. MDR. Denn der MDR-Systembegriff (Art. 2 Nr. 11) verlangt, dass die Kombination selbst einem spezifischen medizinischen Zweck dient. Dass ein KIS einzelne Medizinprodukte-Module enthält, genügt nicht – entscheidend ist, ob der Zweck des Kombinierens ein medizinischer ist. Bei einem KIS ist das typischerweise nicht der Fall: Die Kombination dient der zentralen Informationsverwaltung, nicht der Diagnose oder Therapie.
- Entscheidend ist die Unterscheidung holistisch vs. heterogen. Bei einem holistischen KIS (ein Hersteller, fertig ausgeliefert) fehlt bereits der Akt des „Zusammensetzens“. Bei einem heterogenen KIS (Module verschiedener Hersteller) muss zusätzlich geprüft werden, ob die Kombination einem medizinischen Zweck dient.
- Vorsicht bei der Zweckbestimmung der Kombination! Wird ein heterogenes KIS so kombiniert, dass ein neuer medizinischer Verwendungszweck entsteht, kann dies ein neues Konformitätsbewertungsverfahren auslösen.
1. Ausgangslage
Software-Systeme in Krankenhäusern vereinen häufig Module mit unterschiedlichen Funktionen: reine Datenverwaltung einerseits, diagnostische oder therapeutische Funktionalitäten andererseits. Letztere sind als Medizinprodukt zu qualifizieren. Zusammen bilden diese Module oft ein Krankenhausinformationssystem (KIS).
Lange war unklar, ob ein einzelnes medizinisches Modul das gesamte Software-System zu einem Medizinprodukt macht. Die EuGH-Entscheidung vom 07.12.2017 (C-329/16) schafft Klarheit: Nur die Module, die der Definition eines Medizinprodukts entsprechen, benötigen eine CE-Kennzeichnung.
Doch was bedeutet das für die Einstufung eines KIS als System oder Behandlungseinheit nach der MDR?
2. Was sind Systeme und Behandlungseinheiten?
Die MDR definiert beide Begriffe erstmals legal:
Begriff – Definition nach Art. 2 der EU-Medizinprodukteverordnung (MDR) – Kernelement
- Behandlungseinheit (Nr. 10):
Kombination von zusammen verpackten und in Verkehr gebrachten Produkten für einen spezifischen medizinischen Zweck.
→ Gemeinsame Verpackung erforderlich - System (Nr. 11):
Kombination von Produkten (zusammen verpackt oder nicht), die verbunden oder kombiniert werden, um einen spezifischen medizinischen Zweck zu erfüllen.
→ Zusammensetzen bzw. Kombination erforderlich
Zwei Voraussetzungen sind also entscheidend:
- Akt des Zusammensetzens: Die Produkte müssen tatsächlich kombiniert werden (keine bloße Sachgesamtheit).
- Spezifischer medizinischer Zweck der Kombination: Nicht ein einzelnes Modul, sondern die Kombination als solche muss einem diagnostischen oder therapeutischen Ziel dienen.
Weiterführende Informationen
Lesen Sie hier mehr zum Thema Systeme und Behandlungseinheiten aus Medizinprodukten.
3. Ist ein KIS ein System oder eine Behandlungseinheit?
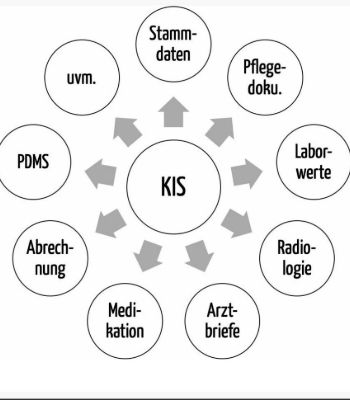
Abb. 1: Ein Krankenhausinformationssystem besteht aus vielen Modulen zum Vergrößern klicken
Holistisches KIS (ein Hersteller, ein Paket)
Liefert ein Hersteller sein KIS als fertiges Gesamtpaket aus, ohne dass jemand Module zusammensetzen muss, liegt weder ein System noch eine Behandlungseinheit vor. Es fehlt bereits der Akt des Zusammensetzens – das KIS wird als fertige Einheit bereitgestellt und in Betrieb genommen.
Heterogenes KIS (Module verschiedener Hersteller)
Werden Module unterschiedlicher Hersteller in einem KIS zusammengeführt, liegt ein Zusammensetzen vor. Dann stellt sich die entscheidende Frage: Dient die Kombination einem spezifischen medizinischen Zweck?
In der Regel: Nein. Ein KIS dient primär der Erfassung, Bearbeitung, Speicherung und Bereitstellung von Informationen. Die medizinischen Module (z. B. ein CDSS) erfüllen ihren medizinischen Zweck jeweils für sich genommen – nicht erst durch die Kombination mit Abrechnungs-, Planungs- oder Archivierungsmodulen.
4. Einordnung der EuGH-Entscheidung
Der EuGH ging in seinem Urteil nicht auf Systeme oder Behandlungseinheiten ein – vermutlich, weil die strittige Software als holistisches System eines einzelnen Herstellers konzipiert war. Die Kernaussage bleibt:
- Nur die medizinischen Module sind zu zertifizieren.
- Der Hersteller muss die Grenzen und Schnittstellen der verschiedenen Module klar angeben. Ein neues Konformitätsbewertungsverfahren wird nur dann erforderlich, wenn Module entgegen ihrer ursprünglichen Zweckbestimmung zu einem neuen System mit medizinischem Verwendungszweck kombiniert werden.
5. Praxistipps
- Zweckbestimmung der Kombination sorgfältig formulieren: Stellen Sie sicher, dass klar erkennbar ist, dass das KIS als Gesamtsystem nicht für diagnostische oder therapeutische Zwecke bestimmt ist – sondern für die zentrale Informationsverwaltung.
- Klare Modulgrenzen definieren: Identifizieren Sie eindeutige Grenzen und Schnittstellen zwischen medizinischen und nicht-medizinischen Modulen – das ist die zentrale Forderung des EuGH.
- Heterogene Konstellationen kritisch prüfen: Sobald Module verschiedener Hersteller kombiniert werden, prüfen Sie, ob durch die Kombination ein neuer medizinischer Zweck entsteht. Falls ja, ist ein Konformitätsbewertungsverfahren erforderlich.
Unterstützung für Sie durch das Johner Institut
Das Johner Institut unterstützt das Medizinprodukte-Ökosystem (Hersteller, Behörden, Benannte Stellen, Betreiber) bei allen regulatorischen Herausforderungen.
- Strategische Beratung
z. B. regulatorische und klinische Strategien für die weltweite Produktzulassung, QM-Systeme, Technische Dokumentation, künstliche Intelligenz - Business Process Outsourcing
z. B. Regularien-Überwachung, Post-Market Surveillance, klinische Bewertung - Software (Enterprise-SaaS)
z. B. für Regularien-Überwachung, Post-Market Surveillance - Produktprüfungen
z. B. Klinische Prüfung, Usability-Prüfungen, Pentesting, Biokompatibilität - Aus- und Weiterbildung
z. B. Seminare, E-Learning (Johner Academy) - Übernahme regulatorischer Rollen
z. B. QM-Beauftragte, Legal-Hersteller, Bevollmächtigte
Quelle: © Johner Institut GmbH
Symbolbild: KI-Illustration, generiert mit ChatCPT/OpenAI