Charité-Studie zeigt Gleichwertigkeit der Software mit bisherigem klinischen Verfahren
Die Tiefe Hirnstimulation (THS) ist ein Therapieverfahren, das zur Behandlung von Parkinson-Erkrankten eingesetzt wird. Zwei im Gehirn implantierte Elektroden stimulieren dabei dauerhaft bestimmte Hirnregionen. Die Einstellung der Stimulationsparameter ist allerdings ein aufwendiger Prozess. Ein Forschungsteam der Charité – Universitätsmedizin Berlin hat nun eine Software entwickelt, die die Einstellung effizienter machen könnte. In ihrer im Fachmagazin The Lancet Digital Health* erschienenen Studie konnten die Forschenden zeigen, dass die softwarebasierte Einstellung im Vergleich zur Stimulationseinstellung des herkömmlichen Verfahrens zu gleichwertigen Ergebnissen in der Verbesserung der motorischen Symptome führt.
Parkinson ist nach Alzheimer die zweithäufigste neurodegenerative Erkrankung. In Deutschland sind etwa 400.000 Menschen betroffen – aufgrund der zunehmenden Alterung der Gesellschaft mit steigender Tendenz. Neben dem als Tremor bezeichneten unwillkürlichen Zittern der Gliedmaßen leiden die Betroffenen insbesondere an Unterbeweglichkeit. „Sie fühlen sich steif, können Bewegungen schlechter starten und beenden, bewegen sich langsamer und haben einen unsicheren Gang, was zu Stürzen führen kann“, sagt Prof. Dr. Andrea Kühn, Leiterin der Sektion Bewegungsstörungen und Neuromodulation an der Klinik für Neurologie mit Experimenteller Neurologie der Charité. „Parkinson ist bislang noch nicht heilbar, doch viele Symptome, insbesondere die schlechte Beweglichkeit, können mit Hilfe der Tiefen Hirnstimulation deutlich verbessert werden.“
Für die Therapieform der Tiefen Hirnstimulation (THS) werden den Patient:innen während eines operativen Eingriffs zwei feine Elektroden ins Gehirn implantiert. Sie geben schwache, kurze elektrische Impulse ab und stimulieren so gezielt und stetig die jeweiligen Hirnregionen. Dafür sind sie über Kabel, die unter der Haut verlaufen, an einen Schrittmacher im Brustraum angeschlossen, über den eine Vielzahl unterschiedlicher Stimulationsparameter eingestellt und individuell an die Symptomatik der Parkinson-Erkrankten angepasst werden können. Drei Monate nach der Operation wird bei den Patient:innen während eines mehrtägigen Klinikaufenthaltes in einem THS-Zentrum die für sie bestmögliche Einstellung ausgetestet. „Die Anpassung der Stimulation erfolgt auf unserer Spezialstation für Bewegungsstörungen durch systematische Testung der Effekte und Nebenwirkungen bei Stimulation der verschiedenen Elektrodenkontakte“, sagt Prof. Kühn. „Um diesen Prozess künftig effizienter und letztlich auch für die Patientinnen und Patienten angenehmer gestalten zu können, haben wir die Software StimFit entwickelt“, sagt Jan Roediger, ebenfalls von der Sektion Bewegungsstörungen und Neuromodulation an der Klinik für Neurologie mit Experimenteller Neurologie und Erstautor der Studie.
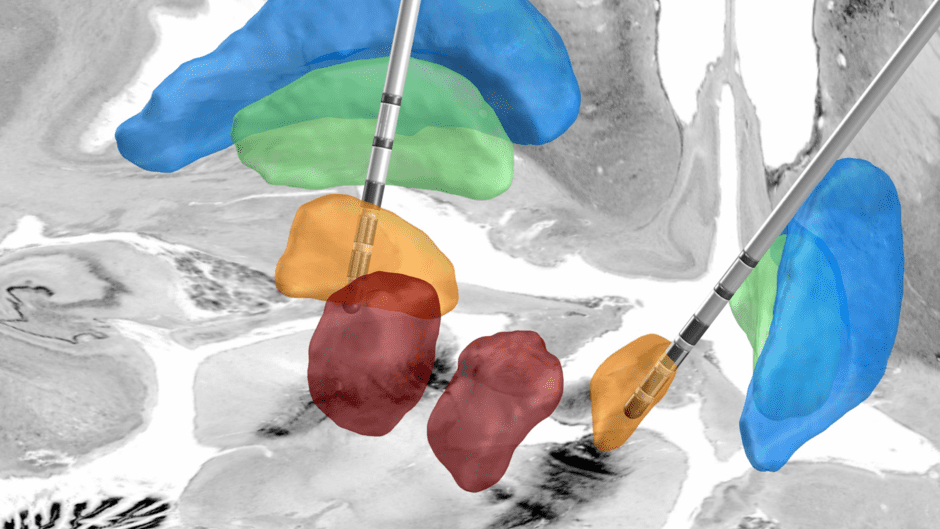
Die Software berechnet auf Basis radiologischer Bilddaten des Gehirns der Patient:innen Vorschläge für eine individuelle Stimulationseinstellung, die zu einer Verbesserung der Symptome führen soll. Zu den wichtigsten Parametern, die dabei berücksichtigt werden, gehört die Stromstärke sowie die genaue Positionierung der stimuliabgebenden Bereiche der Elektroden. „Um die genaue Lage der Elektroden im Gehirn anhand von Bilddaten bestimmen und in den Algorithmus einbeziehen zu können, haben wir die Open-Source-Software Lead-DBS genutzt, die ebenfalls an der Charité entwickelt wurde“, sagt Jan Roediger. „Unser Algorithmus wurde dann mit einem Datensatz aus über 600 Stimulationseinstellungen, den dazugehörigen Bilddaten und Wirkungen auf die Symptomatik trainiert.“
Um zu prüfen, ob die softwarebasierten Einstellungen von StimFit mit denen durch klinisches Austesten gefundenen Einstellungen qualitativ mithalten können, hat das Forschungsteam eine Studie mit 35 Parkinson-Patient:innen durchgeführt. Beide Stimulationseinstellungen – die jeweils individuelle, die durch die herkömmliche klinische Testung erstellt wurde, sowie die softwarebasierte Einstellung – wurden nacheinander getestet. Dabei wussten weder die Studienteilnehmenden noch das Fachpersonal, in welcher Reihenfolge die jeweilige Stimulationseinstellung erfolgte. Im Anschluss wurden die motorischen Symptome nach den beiden Einstellungen beurteilt und miteinander verglichen. „Die allgemeine Beweglichkeit und insbesondere auch das Laufen der Patient:innen verbesserte sich bei beiden Stimulationseinstellungen gleich gut“, sagt Prof. Kühn. „Das ist ein wirklich vielversprechendes Ergebnis. Bildgebungsbasierte Algorithmen könnten die klinische Praxis der THS bei Parkinson und anderen Bewegungsstörungen künftig deutlich vereinfachen und es so ermöglichen, die neuesten technischen Fortschritte – wie etwa Mehrkontaktelektroden zur direktionalen Stimulation – besser zu nutzen.“
Da die Ausprägung der Parkinson-Symptome wie Unterbeweglichkeit, Gangstörungen oder unwillkürliches Zittern (Tremor) bei den Erkrankten individuell unterschiedlich ist und bei der Einstellung der Hirnstimulatoren berücksichtigt werden muss, möchten die Forschenden dies in weiteren Schritten der technischen Optimierung der Software einbeziehen. Sie arbeiten zudem an der Entwicklung von Modellen, die die Wahrscheinlichkeit von Nebenwirkungen genauer vorhersagen können – um die softwarebasierte Stimulationseinstellung und damit den gewünschten künftigen Therapieerfolg zu verbessern und den Weg für weitere klinische Studien zu ebnen.
Über die Studie
Die Studie entstand im Rahmen des neurowissenschaftlichen Charité-Exzellenzclusters „NeuroCure“ und des SFB TRR295 „ReTune“ und wurde durch die Deutsche Forschungsgemeinschaft (DFG) gefördert.
* Roediger J et al. Automated Deep Brain Stimulation programming based on electrode location – a randomized, crossover trial using a data-driven algorithm. The Lancet Digital Health 2022 Dec 15. doi: 10.1016/S2589-7500(22)00214-X
Bild: Die Positionen der Elektroden wurden auf Basis individueller radiologischer Bilddaten ermittelt. Die neu entwickelte Software nutzt diese Informationen, um Vorschläge für effektive Stimulationseinstellungen zu berechnen. Jan Roediger ©Charité
Quelle: Charité – Universitätsmedizin Berlin